Análisis de tendencias, cruciales en los estudios de estabilidad
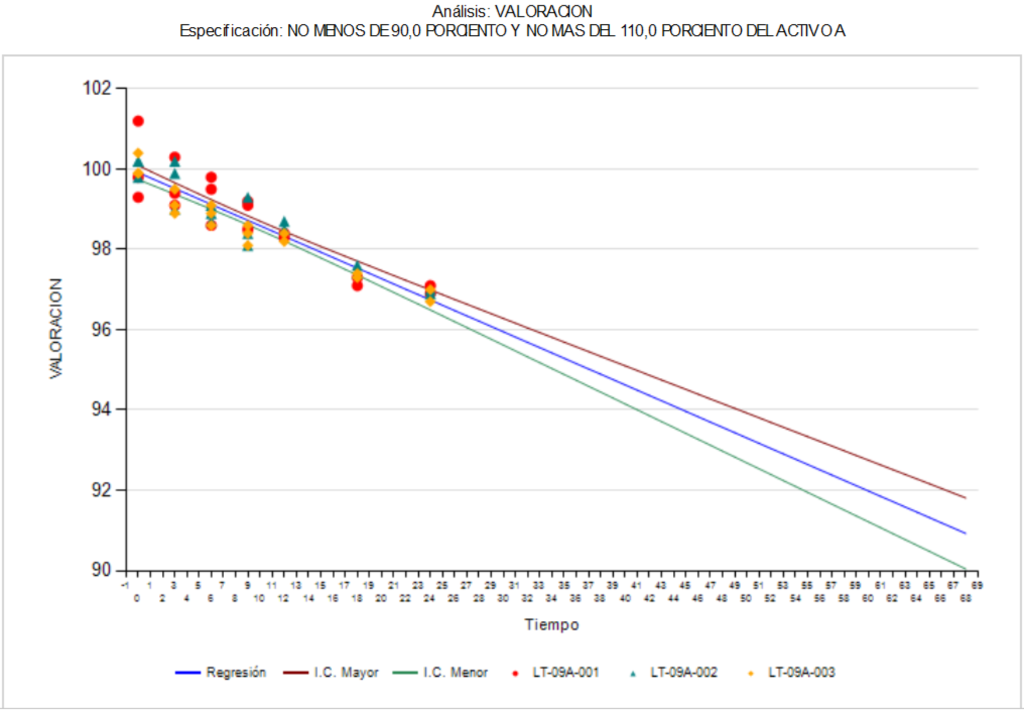
En la industria farmacéutica, el estudio de estabilidad de medicamentos es un proceso esencial para asegurar la calidad, seguridad y eficacia de los productos farmacéuticos. Los estudios de estabilidad se realizan para evaluar cómo cambia la calidad de los medicamentos con el tiempo, en diferentes condiciones de almacenamiento y transporte. Sin embargo, en la actualidad, la importancia de realizar análisis de tendencias en los estudios de estabilidad de medicamentos está tomando cada vez más relevancia, sobre todo para las agencias regulatorias.
Sistematización de los Estudios de Estabilidad y Mejora Continua

Hoy en día es de suma importancia llevar a cabo un control adecuado de los estudios de estabilidad, ya que las entidades regulatorias establecen criterios a cumplir según las normas de cada país e internacionalmente según lo dicta la ICH. La interrogante aquí sería ¿La empresa farmacéutica donde trabaja está cumpliendo con estos criterios?
Cálculos para periodo de reanálisis o vida útil de fármacos y medicamentos

El objetivo de un estudio de estabilidad es conocer que tan estable se mantiene un medicamento en condiciones ambientales definidas, con base en el análisis de mínimo tres lotes del fármaco o medicamento. Por otro lado, también establecer con fundamento estadístico un período de reanálisis o de vida útil, así como conocer las condiciones de almacenamiento indicadas en la etiqueta que aplicarán a los lotes futuros fabricados y envasados en circunstancias similares.
¿Porqué sistematizar los estudios de estabilidad?

Primordialmente, el fabricante de fármacos y/o medicamentos, está obligado a garantizar la calidad, la eficacia y la inocuidad a lo largo de toda la vida útil del producto, con el objetivo de ofrecer al consumidor un producto seguro, y eficaz.
El sistematizar el registro de los estudios de estabilidad, garantiza de manera puntual el documentar los cambios que experimentan las características físico-químicas y microbiológicas del producto.
Combinabilidad de los datos en estudios de estabilidad (Poolability)
Uno de los objetivos del análisis estadístico en los estudios de estabilidad es evaluar si el periodo de reanálisis o vida útil estimado es más largo que el propuesto. Saber si podemos o no combinar los datos de los lotes en la estadística es de vital importancia.
Desviaciones Comunes en Estudios de Estabilidad de Medicamentos
oca
Las desviaciones más comunes en los estudios de estabilidad de medicamentos pueden evitarse utilizando las herramientas adecuadas. Hay desviaciones desde el punto de vista analítico como: incumplimiento de las especificaciones establecidas, material de envase incompatible, fallos en las cámaras climáticas. También existen otras desviaciones administrativas menos severas pero que de igual forma impactan a los estudios de estabilidad
¿Como estimar el periodo de caducidad de medicamentos?
Sin duda alguna, existen varios métodos estadísticos que son de gran utilidad para estimar el periodo de caducidad de un medicamento. En este artículo analizaremos métodos para estudios de estabilidad a largo plazo y a corto plazo.
Registro Sanitario de Medicamentos en México
En México y todos los países desarrollados, el registro sanitario de medicamentos es un trámite obligado para las empresas que los fabrican. Así que es importante conocer como realizar el trámite, su duración y las herramientas técnicas que te ayudarán a facilitarlo.
La Estadística en los Estudios de Estabilidad
La estabilidad de un medicamento puede definirse como el tiempo durante el cual su actividad química y/o biológica y sus características físicas no cambian de forma considerable. Entonces, en los estudios de estabilidad de medicamentos se establecen condiciones extremas a los que un medicamento podría llegar a estar para analizar cual sería su comportamiento físico, químico o biológico.
Estudios de Estabilidad de Medicamentos en México
La estabilidad de un medicamento es la capacidad que tiene un fármaco o medicamento de mantenerse dentro del nivel de calidad que se establece en la etiqueta del envase que lo contiene, al menos durante el periodo de vida útil que le fue aprobado por la autoridad sanitaria, para el caso de México, la COFEPRIS.
Temas
- Aseguramiento de Calidad (3)
- Dispositivos Médicos (3)
- DMSys (2)
- EESys (8)
- Estudios de Estabilidad de Medicamentos (20)
- Grupo DESISA (1)
- Industria Farmacéutica en México (10)
- Mantenimiento del Estado Validado (1)
- RAPSys (11)
- Revisión Anual de Producto (30)
- Sistemas Computarizados en la Farmacéutica (6)
- Validación de Sistemas Computarizados (5)
- Verificación continua del Proceso (6)





