Análisis Oportuno de Muestras de Estabilidad según la NOM-073-SSA1-2015

En la industria farmacéutica, la estabilidad de los productos es un aspecto crítico que garantiza la seguridad y eficacia de los medicamentos a lo largo de su vida útil. La Norma Oficial Mexicana NOM-073-SSA1-2015 establece directrices claras para asegurar que los análisis de estabilidad se realicen de manera adecuada y oportuna. En particular, el punto 10.17 de esta norma indica que “El análisis de las muestras de estabilidad deberá llevarse a cabo durante los 30 días siguientes al retiro de las mismas de las condiciones de estabilidad correspondiente”. Este artículo explora la importancia de este requisito y su impacto en la calidad del producto final.
7 Errores Comunes en Estudios de Estabilidad y Cómo los Sistemas Informáticos Pueden Prevenirlos

En la industria farmacéutica, los estudios de estabilidad son fundamentales para garantizar la seguridad y eficacia de los productos farmacéuticos a lo largo de su vida útil. Sin embargo, la gestión manual de estos estudios puede conducir a errores significativos que afectan la integridad de los datos y, en última instancia, la conformidad regulatoria. A continuación, exploramos los errores más comunes encontrados en las auditorías de estudios de estabilidad y cómo la implementación de sistemas informáticos puede ayudar a prevenirlos.
Análisis de tendencias, cruciales en los estudios de estabilidad
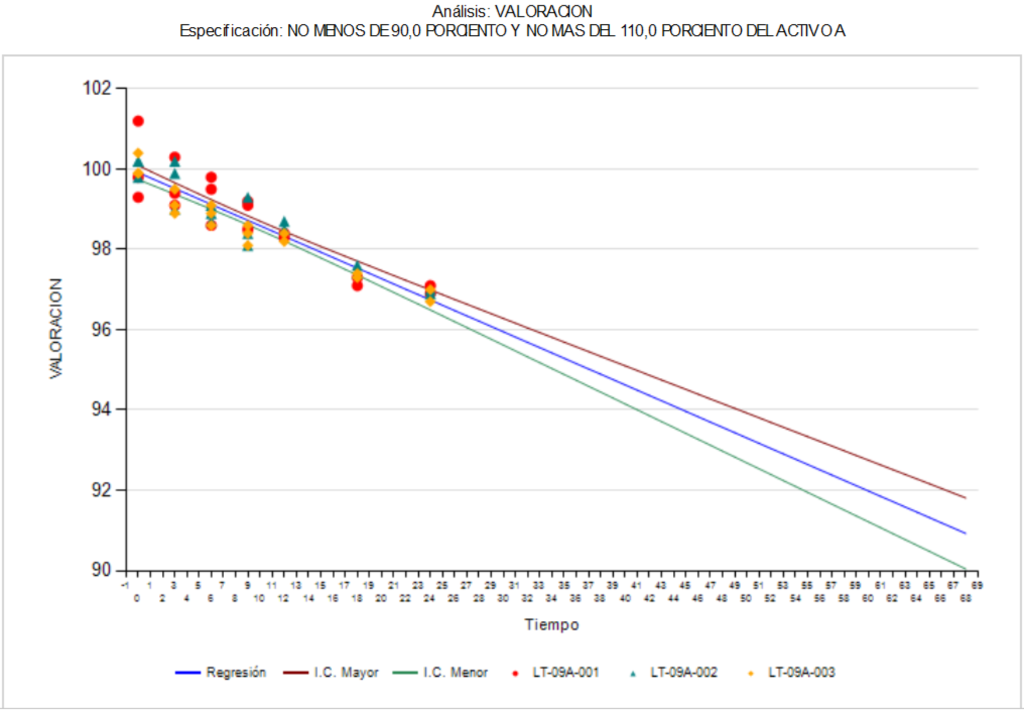
En la industria farmacéutica, el estudio de estabilidad de medicamentos es un proceso esencial para asegurar la calidad, seguridad y eficacia de los productos farmacéuticos. Los estudios de estabilidad se realizan para evaluar cómo cambia la calidad de los medicamentos con el tiempo, en diferentes condiciones de almacenamiento y transporte. Sin embargo, en la actualidad, la importancia de realizar análisis de tendencias en los estudios de estabilidad de medicamentos está tomando cada vez más relevancia, sobre todo para las agencias regulatorias.
¿Porqué sistematizar los estudios de estabilidad?

Primordialmente, el fabricante de fármacos y/o medicamentos, está obligado a garantizar la calidad, la eficacia y la inocuidad a lo largo de toda la vida útil del producto, con el objetivo de ofrecer al consumidor un producto seguro, y eficaz.
El sistematizar el registro de los estudios de estabilidad, garantiza de manera puntual el documentar los cambios que experimentan las características físico-químicas y microbiológicas del producto.
Estudios de Estabilidad de Medicamentos en México
La estabilidad de un medicamento es la capacidad que tiene un fármaco o medicamento de mantenerse dentro del nivel de calidad que se establece en la etiqueta del envase que lo contiene, al menos durante el periodo de vida útil que le fue aprobado por la autoridad sanitaria, para el caso de México, la COFEPRIS.
Temas
- Aseguramiento de Calidad (3)
- Dispositivos Médicos (3)
- DMSys (2)
- EESys (8)
- Estudios de Estabilidad de Medicamentos (20)
- Grupo DESISA (1)
- Industria Farmacéutica en México (10)
- Mantenimiento del Estado Validado (1)
- RAPSys (11)
- Revisión Anual de Producto (30)
- Sistemas Computarizados en la Farmacéutica (6)
- Validación de Sistemas Computarizados (5)
- Verificación continua del Proceso (6)
