El proceso de la revisión anual de producto
En esta cápsula informativa hablaremos sobre el proceso global para realizar la revisión anual de producto o revisión periódica de calidad. Las etapas, el porqué y su importancia.
NOM-241-SSA1-2021 ¡ya es oficial!
El pasado 20 de diciembre de 2021 se publicó en el diario oficial de la federación la nueva NOM-241-SSA1-2021 Buenas prácticas de fabricación para dispositivos médicos…
Nueva Interface Universal para RAPSys© V2

El sistema RAPSys© V2 ahora cuenta con una gran herramienta de Interface Universal (RI) la cual nos permitirá aprovechar el registro de datos realizado en otros sistemas, evitando asi la re-captura de información.
Análisis de tendencias en la revisión anual de producto

En las auditorias realizadas a empresas farmacéuticas por parte de la agencia regulatoria COFEPRIS en México respecto a la revisión anual de producto, una de las oportunidades de mejora más frecuentes reveladas por la misma agencia es “No se realiza análisis de tendencias utilizando herramientas estadísticas“. Así que, en este artículo expondremos una de estas herramientas estadísticas para el análisis de tendencias en la revisión anual de producto.
Revisión periódica de producto – Problemática y Solución

Desafortunadamente aún persiste en algunas empresas de la Industria farmacéutica la problemática referente al proceso “manual” de la Revisión Anual de Producto o revisión periódica de producto. Les presentamos la solución idónea para evitar continuar con estos inconvenientes de integridad de la información.
Nuevo reporte validación etapa 3 – Verificación continua de calidad
Lanzamiento RAPSys© V2.4
El pasado viernes 11 de diciembre de 2020 se les informó a nuestros clientes del lanzamiento de RAPSys© V2.4 el cual contempla como una de sus principales mejoras la incorporación del reporte para la verificación continua de la calidad o validación fase 3. Además de incluir firmas electrónicas para confirmar las modificaciones y eliminación de registros.
Comparar lotes actuales contra el histórico en la RAP

Una de las funciones de aseguramiento de calidad y/o validación es comparar los lotes actuales contra el histórico. Pero ¿que herramientas estadísticas se pueden utilizar para analizar los datos recientes contra su historia?
Grupo Industria Farmacéutica México y LATAM

Grupo DESISA comprometido en apoyar el fortalecimiento tecnológico de la industria farmacéutica de toda América latina y sus colaboradores le invita a formar parte del grupo “Industria farmacéutica en México y LATAM” con el objetivo de crear un espacio de contacto entre profesionales de la industria farmacéutica (Networking) y de compartir información de interés, experiencias, vacantes y posibles colaboraciones (Benchmarking).
Estadística para la verificación continua de la calidad
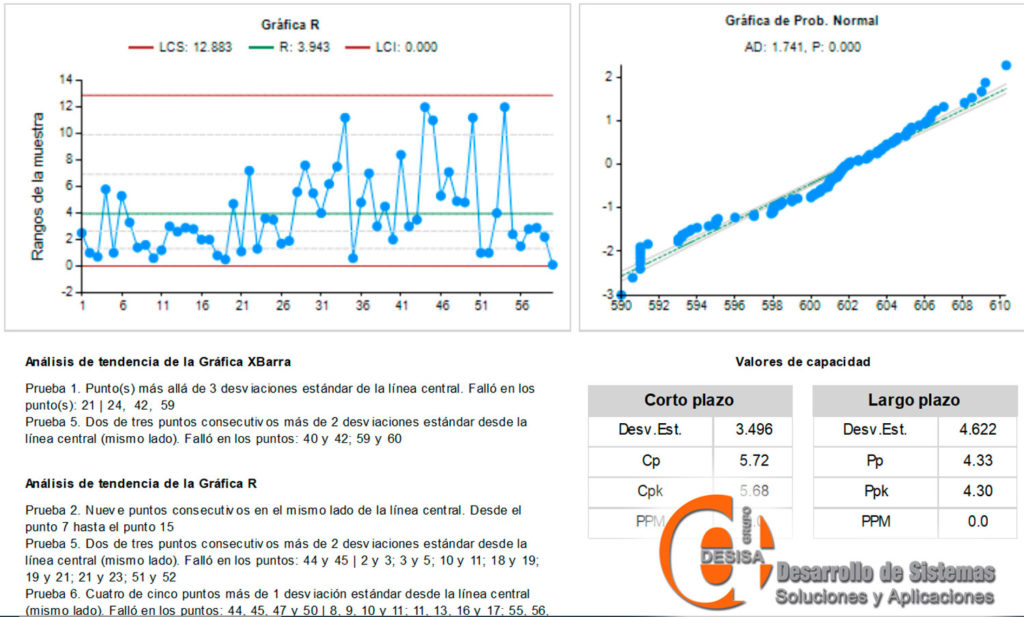
En la actualidad las agencias sanitarias dan mucha importancia al uso de herramientas y métodos estadísticos, a la hora de una inspección sanitaria. Las empresas deben tener disponible los datos reales de la verificación continua del proceso y un sistema estadístico robusto y validable que la sustente.
Cálculos para periodo de reanálisis o vida útil de fármacos y medicamentos
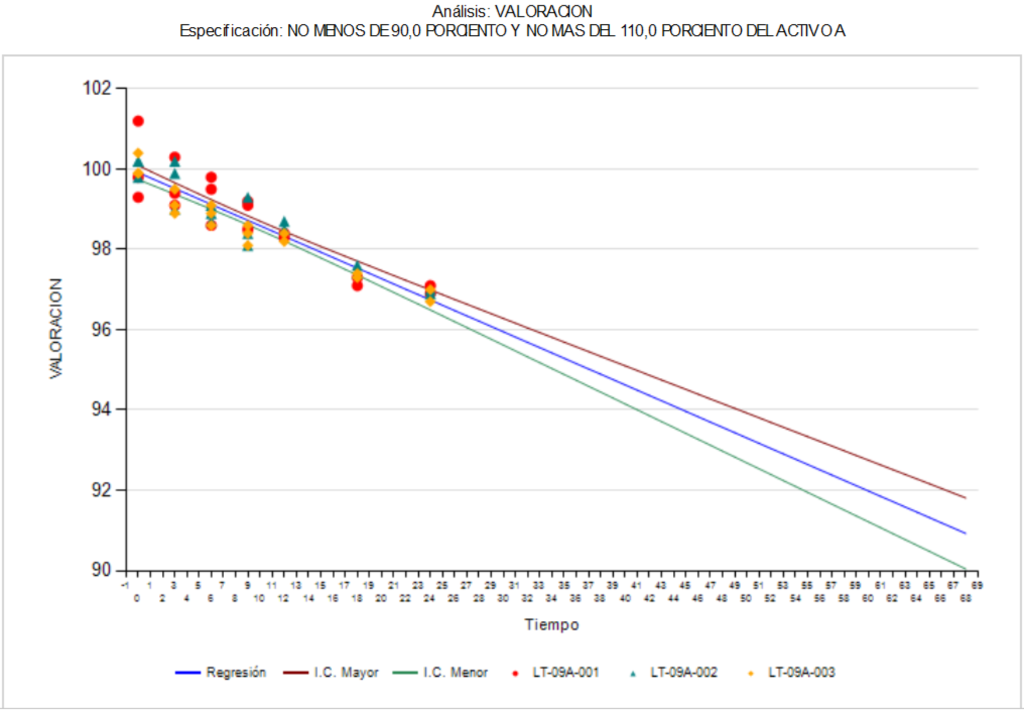
El objetivo de un estudio de estabilidad es conocer que tan estable se mantiene un medicamento en condiciones ambientales definidas, con base en el análisis de mínimo tres lotes del fármaco o medicamento. Por otro lado, también establecer con fundamento estadístico un período de reanálisis o de vida útil, así como conocer las condiciones de almacenamiento indicadas en la etiqueta que aplicarán a los lotes futuros fabricados y envasados en circunstancias similares.
Temas
- Aseguramiento de Calidad (3)
- Dispositivos Médicos (3)
- DMSys (2)
- EESys (8)
- Estudios de Estabilidad de Medicamentos (20)
- Grupo DESISA (1)
- Industria Farmacéutica en México (10)
- Mantenimiento del Estado Validado (1)
- RAPSys (11)
- Revisión Anual de Producto (30)
- Sistemas Computarizados en la Farmacéutica (6)
- Validación de Sistemas Computarizados (5)
- Verificación continua del Proceso (6)

